

06.10 2025
2025年5月29日,Max Planck研究所Meritxell Huch课题组于《Nature》发表最新研究。该研究与之前利用多能干细胞(iPSCs)同时诱导分化获得的肝胆复杂类器官不同,在21年构建的含有胆管细胞和门管间充质细胞(portal fibroblasts)肝脏类器官研究基础上,添加了小鼠肝细胞,建立了一种新的含有肝细胞、胆管细胞与门管间充质细胞的小鼠肝“组装体”(assembloids)系统。该“组装体”不仅有效构建了门管区胆小管(bile canaliculi)网络模拟胆汁排泄,并通过调节间充质细胞比例诱导纤维化样改变,为体外研究胆汁淤积性肝病提供了新的工具,有助于开发新的治疗策略。
背景介绍
肝脏由众多肝脏基本单元肝小叶有机排列构成。肝小叶以中央静脉为轴心,角落分布由肝细胞、胆管细胞及其他细胞组成的门管区。肝细胞,肝脏主要的实质细胞,分泌胆汁至胆小管网络,汇入胆管执行正常生理功能。若胆汁流动或引流发生异常,则会导致胆汁淤积性肝病,并可能进一步发展为纤维化,最终引发肝衰。然而,目前仅有部分工作尝试利用多能干细胞分化获得的肝胆复杂类器官,部分模拟胆汁淤积。体外重现这种多细胞互作及组织结构,将对疾病的发展提供新视角。
研究思路与方法
1、 构建具有功能性胆小管网络的肝细胞类器官(HepOrg)
由于胆汁排泄的功能依赖于有功能的胆小管网络,研究团队首先优化了培养基成分在肝细胞类器官诱导三维胆小管网络的出现。该团队发现培养基添加Wnt3a及Wnt surrogate可促进葡萄状类器官形成。该类器官不仅维持了肝细胞特征标志物的表达及功能维持,还形成了生理的胆小管结构并可将胆汁酸模拟物转运至胆小管腔。为了实现后续肝细胞类器官与胆管细胞及门管区间充质细胞共培养,该团队进一步优化培养基成分。有意思的是,该研究团队在优化后的肝细胞类器官培养基中发现减少Wnt信号刺激后,肝细胞类器官部分门管区(zone1)基因上调(通常认为Wnt信号对于肝细胞中央静脉区(zone3)基因表达具有促进作用)。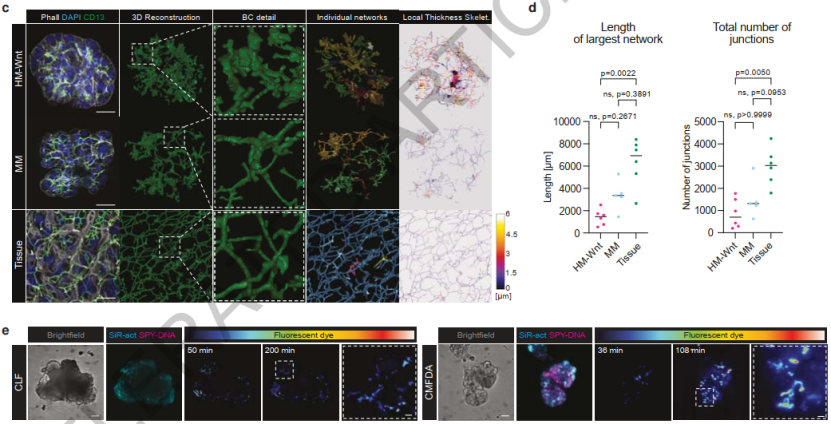
2、 利用肝细胞类器官、胆管细胞及门管区间充质细胞构建组装体
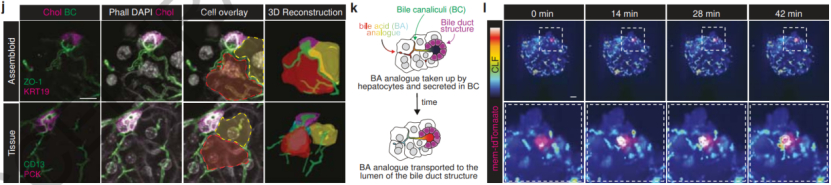
胆汁排泄需要肝细胞分泌胆汁经胆小管网络排泄至胆管内。研究团队将优化后的肝细胞类器官与胆管细胞及门管区间充质细胞按比例混合,在Rocking平台或者Aggrewell聚合。48h内,胆管细胞可迁移至肝细胞类器官内部并被门管区间充质细胞包裹与体内门管区结构高度类似。使用胆汁酸模拟物CLF成像证明了胆小管与胆管功能性连接。该结果为后续研究提供了稳定的体外模型。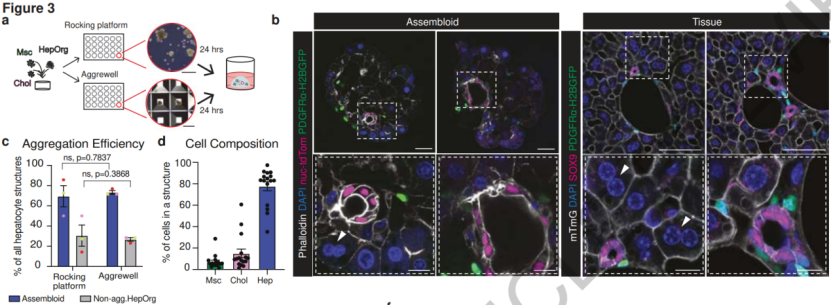
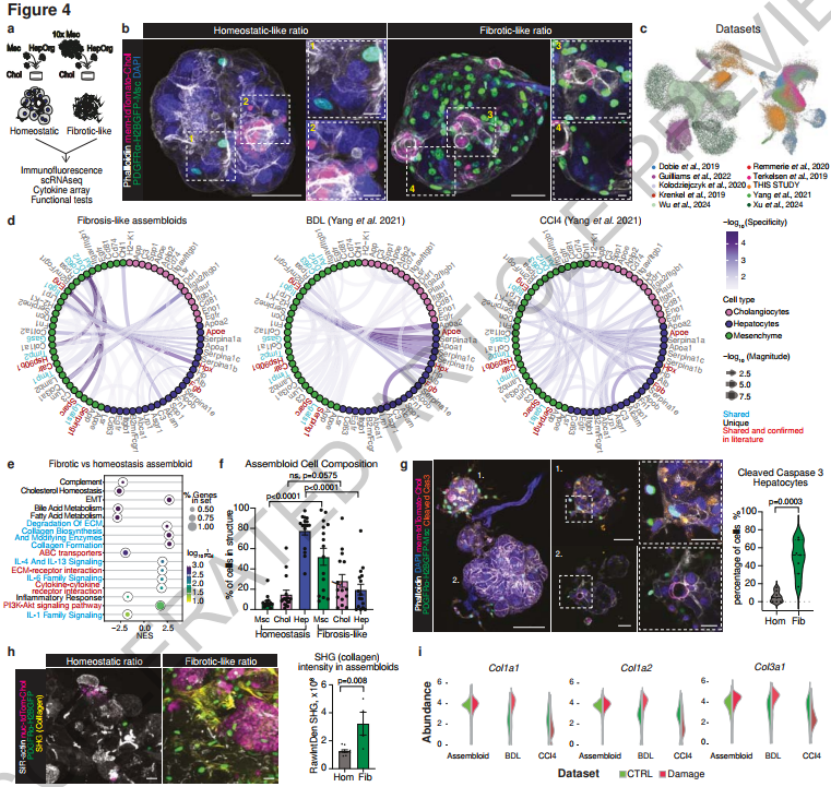
3、 调节门管区间充质细胞比例模拟胆道纤维化
为了模拟胆道纤维化,该研究团队将门管区间充质细胞比例提高10倍,建立纤维化模型。有意思的是,在无任何免疫细胞的存在下(通常认为免疫细胞对于肝脏纤维化的发生发展具有重要作用),纤维化模型下的组装体结构紧密,纤维化相关基因表达上调,胶原沉积显著。肝细胞发生凋亡,转录组水平提示肝向胆管谱系的转变。此外胆管细胞增殖明显,与纤维化病人出现的胆管反应中胆管细胞数量增多对应。总的来说,该模型重现了胆汁淤积性肝纤维化过程中的部分病理特征。
4、 利用胆汁淤积小鼠模型的肝细胞类器官构建的组装体,模拟纤维化的病理状态
为了模拟纤维化肝脏的病理特征,研究团队利用Mdr2-/-基因敲除小鼠构建的肝细胞类器官重现了体内胆汁淤积的重要表型包括胆小管扩张、顶端隔板结构、内陷性泡状突起及肝玫瑰花结构积聚。进一步将胆汁淤积性肝细胞类器官与野生型胆管细胞及门管区间充质细胞混合,构建的嵌合组装体表现出胆管细胞扩张,类似于胆管纤维化的早期阶段。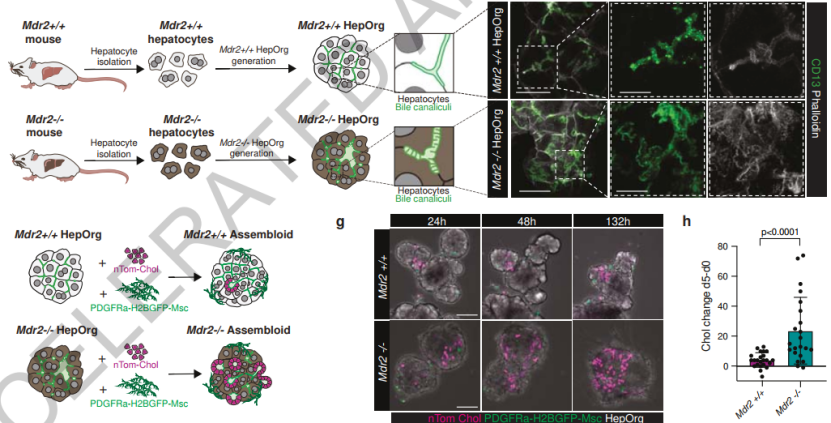
总结与思考
总的来说该团队首次利用三种肝组织细胞构建了门管区组装体,以精美的图像数据展示了之前研究未能达到的接近生理的胆小管网络结构及功能。为肝脏复杂类器官的构建提供了一种新思路。
尽管该组装体模型取得了众多突破,但仍有需要值得我们思考的部分。除了文中提到的局限性包括未能实现肝小叶的代谢分区建立及缺乏免疫微环境外,在组装体构建过程中,阐释什么信号trigger了胆管细胞与肝细胞类器官识别连接,可能对未来构建更加可控的门管区复杂类器官具有指导作用。此外,采用临床可能诱导胆道纤维化的药物刺激组装体可能比单纯的提高门管区间充质细胞的比例更容易让人理解。
早在2018年,Hans Clevers团队建立了人胎儿肝细胞类器官的长期扩增培养条件,并提供了在人肝导管类器官和人胎儿肝细胞类器官中进行CRISPR - Cas9基因组工程的策略。
关于胎肝类器官
胎肝类器官在产业化建库存在关键优势,拥有更好的扩增能力和基因编辑的可行性。
第一,胎肝类器官模型成功率超90%,均能够长期稳定传代。对于生长因子,如Wnt信号的响应更高效,在体外容易达成代谢与增殖的平衡,能为药物的肝毒性测试搭建系统性平台。
第二,胎肝类器官能模拟肝细胞的发育过程,揭示肝细胞分化和成熟的关键信号通路,为各类肝病的发生和发展研究提供可靠模型。
第三,更易通过CRISPR技术实现基因编辑,例如模拟个体间遗传变异(PNPLA3I148M)或单基因脂质紊乱(APOB和MTTP突变),建立脂肪肝疾病模型。
目前,丹望医疗在人胎肝类器官领域的前瞻性布局已进入加速落地阶段。依托国际顶尖研发团队及全球领先的消化道类器官技术平台积累,公司正加速推进胎肝类器官研发管线的技术转化与产业化进程!


